Làm mờ ranh giới vô cơ - hữu cơ
Sau khi lý thuyết về cấu trúc hóa học do Kekulé đưa ra và được hoàn thiện bởi các nhà hóa học hàng đầu châu âu vào những năm 50 của thế kỷ 18(1), cấu trúc của các chất hữu cơ với bộ khung của các nguyên tử carbon hóa trị 4 do carbon tạo liên kết cộng hóa trị bằng cách góp 4 điện tử với các nguyên tử gần kề có thể được coi như một học thuyết(2).
Carbon, trong "tâm khảm" luôn được coi là nguyên tố phi kim có hóa trị 4.
Chỉ cách đây vài ngày, trong một công bố của Alois Fürstner cùng các đồng nghiệp tại Viện Max Planck nghiên cứu các hợp chất carbon (Max-Planck-Institut für Kohlenforschung) thuộc thành phố Mülheim (CHLB Đức) cho rằng khả năng carbon mang đặc điểm của một kim loại cao hơn nhiều so với chúng ta đã từng nghĩ về nó.
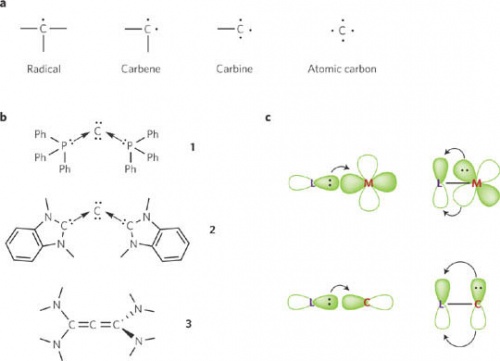
Các tác giả cho rằng trong một số chất mới được tổng hợp và cả trong những chất đã tồn tại, carbon có khả năng cho và nhận đôi điện tử từ những nguyên tử lân cận - đặc tính của các ion kim loại mang điện tích dương.
Tính chất đặc biệt này làm mờ ranh giới giữa hóa vô cơ và hóa hữu cơ và có thể làm nền tảng cho sự ra đời của thế hệ chất xúc tác mới.
Nghiên cứu được công bố trên Nature Chemistry (Nature Chemistry 1, 295 - 301 (2009).
Tham khảo[sửa]
1. Alan J. Rocke. Series The Cambridge History of Science, Volume 5 The Modern Physical and Mathematical Sciences, Chapter Title 13: The Theory of Chemical Structure and its Applications .
2. C. Adam Dyker & Guy Bertrand. Chemical bonding: Rethinking carbon. Nature Chemistry 1, 265 - 266 (2009).





