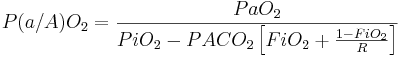Đánh giá chức năng phổi sơ sinh
BS. Võ Đức Minh
Đo các chỉ số khí máu là phương pháp lâm sàng được sử dụng rộng rãi nhất để đánh giá chức năng phổi ở sơ sinh và tạo cơ sở để chẩn đoán và điều trị bệnh tim phổi. Bài này biện luận vì sao những thay đổi về áp suất riêng phần của oxy trong phế nang (Áp suất riêng phần của oxy trong phế nang) và PACO2 phản ánh chức năng phổi bị rối loạn trong các tình huống lâm sàng khác nhau.
Các giá trị PAO2 và PACO2 phụ thuộc vào thành phần và thể tích của khí phế nang, thành phần và thể tích của máu tĩnh mạch hổn hợp và các cơ chế tổn thương sự trao đổi khí phổi. Thành phần khí phế nang có thể tính được dựa vào phương trình
Trong đó PiO2 là áp suất riêng phần của khí oxy hít vào (PiO2 = FiO2 x [áp suất khí quyển – áp suất hơi nước]). Ngang mực nước biển, áp lực khí quyển là 760 mmHg; với độ ẩm 100%, áp lực hơi nước là 47 mmHg. Khí trời bình thường có FiO2 là 0,21. Do đó PiO2 = 0,21 x (760-47) mmHg ≈ 150 mm Hg. PACO2 là áp lực riêng phần của dioxide carbon trong phế nang và R là thương số hô hấp (thường là 0,8). Thương số hô hấp là một số không có đơn vị, được sử dụng trong các phép tính về tốc độ chuyển hóa cơ bản. Thương số hô hấp = CO2 sản xuất / O2 tiêu thụ
Ngang mực nước biển, thở khí trời: PAO2 = 150 mmHg – 1,2 PACO2
Các cơ chế gây tổn thương trao đổi khí phổi bao gồm bất tương xứng thông khí/tưới máu phổi (V ̇/Q ̇) (tỷ lệ thông khí/tưới máu bình thường là 0,8), shunt, giảm thông khí và sự khuyếch tán bị giới hạn. Sự phù hợp của khí máu phế nang và máu tĩnh mạch hổn hợp mang lại trao đổi khí tối ưu. Thành phần và các thể tích máu tĩnh mạch hổn hợp được xác định bởi thành phần khí máu động mạch, cung lượng tim, sự tiêu thụ oxy và sự sản xuất dioxide carbon (CO2).
Mục lục
Áp suất riêng phần của oxy động mạch[sửa]
Phụ thuộc vào hiệu lực của trao đổi khí, áp suất riêng phần của oxy trong phế nang (sức căng) nhằm cân bằng với máu tĩnh mạch hổn hợp, tạo ra PaO2, xác định được mức độ bão hòa oxy của hemoglobin. Cùng với sự kết hợp hóa học với hemoglobin, oxy cũng hòa tan trong plasma và hồng cầu. Hầu hết oxy trong toàn bộ máu kết hợp với hemoglobin (được đo trên lâm sàng như là bão hòa oxy), trong khi số lượng oxy hòa tan chỉ là một tỷ lệ nhỏ của toàn bộ số lượng được mang trong máu.
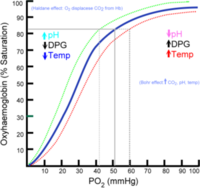
Số lượng oxygen kết hợp với hemoglobin phụ thuộc vào PaO2 và đường cong phân ly oxy (Hình 1). Máu hầu như được bão hòa hoàn toàn khi PaO2 từ 90 đến 100 mmHg. Phần phẳng của phần trên của đường cong phân ly hình chữ S hầu như không thể xác định được sức căng của oxy lớn hơn 60-80 mmHg nếu như chỉ sử dụng độ bão hòa oxy động mạch. Đường cong phân ly của hemoglobin thai (khi so sánh với hemoglobin người lớn) di chuyển về trái và nếu PaO2 dưới 100 mmHg, máu thai kết hợp nhiều oxy hơn. Sự di chuyển này dường như do ái lực thấp hơn của hemoglobin thai với 2,3 diphosphoglycerate. Chú ý rằng pH, PaCO2, nhiệt độ và nồng độ của diphosphoglycerate ảnh hưởng vị trí của đường cong phân ly.
Hình 1: Đường cong phân ly O2-hemoglobin biểu hiện mối liên quan giữa nồng độ oxy và độ bão hòa phần trăm của Hb. Khi nồng độ tăng trên 90% đường cong trở nên phẳng.
Bảng 1: Có nhiều yếu tố ảnh hưởng đến sự kết hợp này và thay đổi hình dạng của đường cong phân ly:
| Di chuyển về phải | Di chuyển về trái | |
|---|---|---|
| Nhiệt độ | Cao | Thấp |
| Diphosphoglycerate | Cao | Thấp |
| PaCO2 | Cao | Thấp |
| pH | Thấp (nhiễm toan) | Cao (nhiễm kiềm) |
| Loại hemoglobin | Hemoglobin người lớn | Hemoglobin thai |
Nồng độ của oxy động mạch (CaO2) là tổng của oxy kết hợp hemoglobin và oxy hòa tan, được mô tả bằng phương trình sau:
CaO2 = (1,37 x Hb x SaO2) + (0,003 x PaO2)
Trong đó nồng độ oxy động mạch được tính bằng mL/100mL của máu, 1,37 là lượng oxy (tính bằng millilit) kết hợp với 1g hemoglobin ở độ bão hòa 100%, Hb là nồng độ hemoglobin (g/100mL), SaO2 là tỷ lệ phần trăm của hemoglobin kết hợp với oxygen và 0,003 là chỉ số tan của oxy trong plasma (tính bằng mL/mm Hg). Trong phương trình này, biểu thức đầu tiên (1,37 x Hb x SaO2) là số lượng oxy kết hợp với hemoglobin. Biểu thức thứ hai (0,003 x PaO2) là số lượng oxy hòa tan trong plasma và trong hồng cầu.
Hầu hết oxy trong máu được vận chuyển bởi hemoglobin. Chẳng hạn, nếu một đứa bé có PaO2 80 mm Hg, SaO2 là 99% và nồng độ hemoglobin là 15 g/100 mL, CaO2 là tổng số của oxy kết hợp với hemoglobin ([1,37 x 15 x 99]/100 = 20,3 mL) cộng với oxy hòa tan trong plasma (0,003 x 80 = 0,24 mL). Trong ví dụ này, chỉ trên 1% oxy trong máu được hòa tan trong plasma và hầu hết 99% được vận chuyển bởi hemoglobin.
Áp suất riêng phần của oxy trong máu động mạch không chỉ phụ thuộc vào khả năng phổi di chuyển oxy được xác định bởi thông khí phế nang mà còn phụ thuộc phần lớn vào tỷ lệ thông khí/tưới máu phổi (V ̇/Q ̇). Để trao đổi khí bình thường sự thông khí và sự tưới máu phổi phải tỷ lệ thuận. Tỷ lệ này rất gần 1:1; đó là, cứ mỗi millilit khí qua phế nang, sẽ phải có một thể tích tỷ lệ máu trong giường mao mạch phổi. Nếu V ̇/Q ̇ giảm (như trong Bệnh màng trong sơ sinh), chỉ một phần được oxy hóa và CO2 tách khỏi máu tĩnh mạch hổn hợp xảy ra. Cần phải bổ sung oxy để khắc phục tình trạng giảm oxy máu khi tỷ lệ V/Q giảm. Nếu tỷ lệ V/Q cao, như trong trường hợp tăng thông khí, áp suất riêng phần của oxy tăng nhẹ.
Cơ chế của shunt trở nên hiển nhiên khi máu đi tắt qua phế nang, xảy ra trong bệnh tim bẩm sinh có tím, tồn tại tuần hoàn thai hoặc xẹp phổi. Bổ sung oxy không ngăn ngừa được tình trạng giảm oxy máu do những shunt như vậy tạo ra. Giảm thông khí (ví dụ do ngưng thở) là nguyên nhân phổ biến của tình trạng giảm oxy máu. Sự hạn chế khuyếch tán có thể ảnh hưởng nhẹ đến oxy hóa nhưng cơ chế này không phải là nguyên nhân phổ biến của tình trạng giảm oxy máu nặng ở trẻ sơ sinh. Giảm oxy máu do hoặc là giảm thông khí hoặc là hạn chế khuyếch tán có thể được điều trị dễ dàng bằng bổ sung oxy.
Ba chỉ số có thể được sử dụng để đánh giá mức độ oxy hóa rối loạn. Tỷ số áp lực oxy động mạch-phế nang (tỷ số PaO2/PAO2 hoặc a/AO2) không có đơn vị, giảm nếu tình trạng oxy hóa giảm, và có thể được xác định bằng phương trình
![P(a/A)O_{2}={\frac {PaO_{2}}{PiO_{2}-PACO_{2}\left[FiO_{2}+{\frac {1-FiO_{2}}{R}}\right]}}](https://tusach.thuvienkhoahoc.com/images/math/2/b/b/2bb6a1d0c7bcde58cac41f4e41adb979.png)
Trong đó R là thương số hô hấp. Vì [R x FiO2 + (1-FiO2)] gần bằng 1 và PACO2 gần bằng PaCO2, phương trình này có thể được đơn giản như sau:
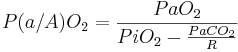
Độ chênh áp oxy phế nang-động mạch (PAO2-PaO2 hoặc AaDO2) được biểu hiện bằng millimet thủy ngân, tăng khi tình trạng oxy hóa bị xấu đi và có thể xác định bằng phương trình sau:
![P(A-a)O_{2}=PiO_{2}-PACO_{2}\left[FiO_{2}+{\frac {1-FiO_{2}}{R}}\right]-PaO_{2}](https://tusach.thuvienkhoahoc.com/images/math/b/a/1/ba11c238509e3639928fd75ad5269030.png)
Hoặc
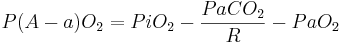
Tỷ số oxy hóa được biểu hiện bằng millimet thủy ngân, giảm nếu tình trạng oxy hóa xấu đi và có thể xác định bằng phương trính
Tỷ
số
oxy
hóa
=
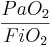
Tỷ số oxy hóa thường ít được sử dụng vì nó đánh giá không chính xác sự rối loạn oxy hóa khi PaCO2 thay đổi đáng kể.
Thường cần thiết điều chỉnh mức độ oxy hóa cho hổ trợ thông khí vì tình trạng oxy hóa bị ảnh hưởng mạnh bởi áp lực đường thở trung bình (P ̅aw hoặc MAP) trong quá trình thông khí hổ trợ. Chỉ số oxy hóa (OI) có ích trong các trường hợp này. OI, tăng trong trường hợp tình trạng oxy hóa xấu đi hoặc tăng P ̅aw, có đơn vị centimet nước mỗi millimet thủy ngân và cò thể xác định bằng phương trình
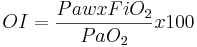
Áp suất riêng phần của Dioxid Carbon (CO2) động mạch[sửa]
PaCO2 là một tiêu chuẩn quan trọng đánh giá chức năng phổi trong bệnh hô hấp sơ sinh. Các cơ chế nguyên nhân của rối loạn trao đổi CO2 của phổi bao gồm giảm thông khí, bất tương xứng V ̇/Q ̇ và shunt. Thêm vào đó, sự gia tăng khoảng chết, xảy ra trong trường hợp phế nang giãn quá mức hoặc bẩy khí làm xấu đi tình trạng thải CO2. Vì hệ số tan của CO2 cao, sự hạn chế khuyếch tán hiếm khi ảnh hưởng sự trao đổi CO2. Nồng độ CO2 trong mô cao hơn so với trong máu động mạch, các phân tử khuyếch tán vào mao mạch và được vận chuyển trong hồng cầu và plasma. Không giống như đường cong phân ly hình chữ S của O2, mối liên quan giữa áp lực CO2 và nồng độ hầu như tuyến tính trên giới hạn sinh lý.
Bắt
đầu
thông
khí
bằng
nhịp
thở
đầu
tiên
sau
sinh
thường
gây
ra
sự
giảm
nhanh
chóng
PaCO2
trong
vài
phút
sau
sinh.
PaO2
tăng
nhanh
đến
mức
60
đến
90
mm
Hg,
mặc
dù
có
một
mức
độ
không
tương
xứng
V
̇/Q
̇
rõ
trong
1
đến
2
giờ
đầu
tiên
của
cuộc
sống.
Người
ta
tin
rằng
điều
này
do
kết
quả
của
shunt
phải-trái
trong
tim
và
phổi.
Ảnh
hưởng
của
sự
thích
nghi
đột
ngột
này
trong
khí
máu
được
minh
họa
trong
hình
2,
cho
thấy
sự
thay
đổi
nhanh
PaO2
và
PaCO2
trong
những
điều
kiện
bình
thường
và
khi
có
ngạt
chậm
có
nhịp
thở
đầu
tiên.
Tốc
độ
mà
thông
khí
và
tưới
máu
phổi
được
phân
bố
đồng
đều
chứng
tỏ
khả
năng
đáng
kể
của
trẻ
sơ
sinh
có
khả
năng
duy
trì
huyết
động.
Hình 2: Những thay đổi PaO2 và PaCO2 trong những phút đầu tiên sau khi sinh (minutes after birth) ở một trẻ bình thường (A) và ở một trẻ bị ngạt (B) có khởi phát hô hấp bị chậm.
Thử nghiệm Tăng oxy-Tăng thông khí[sửa]
Thử nghiệm tăng oxy được thực hiện bằng cách đặt bệnh nhân vào trong môi trường có nồng độ oxy 100% trong 5 đến 10 phút và sau đó thử khí máu động mạch hoặc theo dõi không xâm nhập tình trạng oxy hóa. Sinh lý cơ bản của phương pháp này là sau 5 đến 10 phút tiếp xúc với oxy sẽ khuyếch tán oxy đến ngay cả những vị trí được thông khí kém và cải thiện tính trạng oxy hóa. Nếu tình trạng giảm oxy máu vẫn tồn tại sau khi tiếp xúc với oxy 100% gợi ý rằng có shunt phải-trái vì tình trạng oxy hóa cải thiện chỉ ở những bệnh nhân bị bệnh phổi nguyên phát. Thử nghiệm này giúp phân biệt giữa bệnh phổi nguyên phát và bệnh tim bẩm sinh có shunt phải-trái.
Cải tiến thử nghiệm tăng oxy kết hợp giữa tăng oxy và tăng thông khí có thể được sử dụng để phân biệt giữa bệnh tim bẩm sinh cấu trúc và tăng áp phổi tồn tại (hoặc nguyên phát) ở trẻ sơ sinh (PPHN), cả hai bệnh này đều có shunt phải-trái. Thở oxy 100% cải thiện tình trạng oxy hóa ở một số bệnh nhân bị PPHN.
Đáp ứng với tăng thông khí với oxy 100% (PaCO2 25 đến 30 mm Hg), nhiều bệnh nhân bị PPHN cải thiện được Pao2 cao hơn 100 mm Hg.
ĐÁNH GIÁ SHUNT[sửa]
Khi có shunt phải-trái qua ống động mạch máu chưa bão hòa từ bên phải của tim vào động mạch phổi chính và qua ống động mạch vào động mạch chủ xuống. Vì ống động mạch hầu như luôn luôn vào động mạch chủ tại vị trí phía sau gốc của các động mạch dưới đòn phải và động mạch cảnh phải, máu đến hai động mạch này được oxy hóa tốt, trong khí các mẫu máu từ động mạch chủ và thường là động mạch dưới đòn trái ít được oxy hóa hơn nếu có shunt phải-trái. Như vậy, khí máu trước ống có thể được lấy từ động mạch quay phải, trong khi máu trong động mạch chủ xuống và thường động mạch quay trái có nguồn gốc sau ống. Giải pháp thay thế, đặt hai dụng cụ đo độ bão hòa oxy (một ở bàn tay phải và một ở bàn tay trái hoặc một trong hai bàn chân) đạt cùng hiệu quả để phân biệt PaO2 hoặc độ bão hòa oxy trước ống và sau ống.
Các bệnh nhân bị PPHN thường có shunt phải-trái qua lỗ bầu dục và qua ống động mạch. Shunt qua ống động mạch có thể được thể hiện bằng sự hiện diện sự chênh lệch oxy hóa đồng thới giữa máu động mạch trước ống và sau ống, trong khi shunt qua lỗ bầu dục ảnh hưởng tình trạng oxy hóa cả trước ống và sau ống. Siêu âm tim có thể được sử dụng để xác định các shunt lỗ bầu dục và ống động mạch.
CÁC TRỊ SỐ ĐO SINH LÝ[sửa]
Các thử nghiệm chức năng phổi được thực hiện ở trẻ sơ sinh bị bệnh có thể giúp chẩn đoán và điều trị. Đánh giá X quang ngực là một phần không thể thiếu trong chẩn đoán các bệnh hô hấp. Các trị số đo áp lực tĩnh mạch trung tâm và áp lực động mạch phổi có thể cung cấp thông tin hữu ích gián tiếp liên quan chức năng phổi nhưng hiếm khi thực hiện được trong bối cảnh lâm sàng sơ sinh. Các trị số đo về lưu lượng khí, thể tích và áp lực được sử dụng để tính cơ học và năng lượng phổi có thể được sử dụng để phân biệt các thực thể bệnh và hướng dẩn điều trị. Các định lượng thời gian thực và biểu đồ x-y của lưu lượng khí, thể tích và các áp lực có thể rất hữu ích tại giường bệnh.
Lưu lượng khí[sửa]
Có nhiều dụng cụ đánh giá lưu lượng khí ở trẻ nhỏ. Các dụng cụ không thâm nhập có thể được sử dụng trong các giai đoạn dài, mang lại các chỉ số đo định tính về lưu lượng đủ để theo dõi tim phổi. Tuy nhiên, các chỉ số định lượng hiện nay cần dụng cụ xâm nhập như là lưu tốc kế hô hấp (pneumotachometer), thiết bị đo tốc độ khí có dây nóng (hot wire anemometer) hoặc lưu lượng kế siêu âm (ultrasonic flowmeter) để phân tích chính xác cơ học phổi.
Lưu tốc kế hô hấp là tiêu chuẩn vàng để đo định lượng lưu lượng khí. Thiết kế cơ bản bao gồm một bộ phận có điện trở như là một màng hình mắt lưới hoặc một vật liệu khác giữa hai hình trụ. Khi không khí thổi qua bộ phận có điện trở, sự giảm áp lực xảy ra có thể đo được cung lượng trong các đơn vị khí thổi. Tín hiệu dòng thổi có thể tích hợp để đạt được VT. Để đo chính xác dòng thổi, tất cả không khí phải qua lưu tốc kế hô hấp. Như vậy, ở một bệnh nhân được thông khí lưu tốc kế hô hấp có thể được gắn vào ống nội khí quản, giảm thiểu sự dò khí bằng cách sử dụng ống nội khí quản có bong chèn hoặc ấn nhẹ vào cổ. Sự khác biệt giữa thể tích thở vào và thở ra là số lượng khí bị dò. Ở bệnh nhân tự thở được, lưu tốc kế hô hấp phải được gắn vào mặt nạ mũi hoặc miệng được gắn kín quanh mũi và miệng bệnh nhân.
Trong thực hành lâm sàng phương pháp định tính phổ biến nhất để đo lưu lượng khí là theo dõi trở kháng. Trở kháng được đo sử dụng hai điện cực đặt mỗi bên lồng ngực. Theo dõi trở kháng dựa vào nguyên lý không khí có trở kháng cao hơn so với mô. Sử dụng một dòng điện rất nhỏ đi qua cơ thể, các điện cực có thể phát hiện sự gia tăng trở kháng khi tỷ lệ không khí-mô thay đổi khi không khí vào phổi trong quá trình gắng sức thở vào. Mặc dù trở kháng có khả năng tối thiểu để định lượng biên độ thở thật sự khi so sánh bằng lưu tốc kế hô hấp, nó có thể phát hiện sự ngưng lưu lượng khí và như vậy phát hiện sự cố ngưng thở trung tâm. Tuy nhiên, vì không khí có thể di chuyển tới lui trong khoang lồng ngực trong khí tắt nghẽn đường thở, trở kháng không thể phân biệt ngưng thở do tắt nghẽn với hô hấp bình thường.
Các chỉ số đo định tính lưu lượng khí cũng có thể thực hiện tại mũi qua một nhiệt kế điện tử hoặc máy phân tích CO2 cuối kỳ thở. Nhiệt kế điện tử phát hiện sự gia tăng nhiệt độ khi không khí ấm từ cơ thể đi qua cái cảm biến trong quá trình thở ra, trong khi trong quá trình thở vào không khí từ khí quyển làm mát cái cảm biến trở về nhiệt độ phòng. Máy phân tích CO2 cuối kỳ thở ra đo nồng độ CO2 trong quá trình thở ra cũng có thể được sử dụng như dụng cụ cảm biến luồng khí. Mặc dù cả hai dụng cụ phát hiện CO2 cuối kỳ thở ra và nhiệt kế điện tử đã được sử dụng để ghi nhận sự giảm hô hấp, cả hai đều liên quan kém với độ lớn của VT. Tuy nhiên, những dụng cụ này có thể được sử dụng cùng với theo dõi trở kháng để phân biệt ngưng thở trung tâm ngược lại với tắc nghẽn.
Thế tích phổi[sửa]
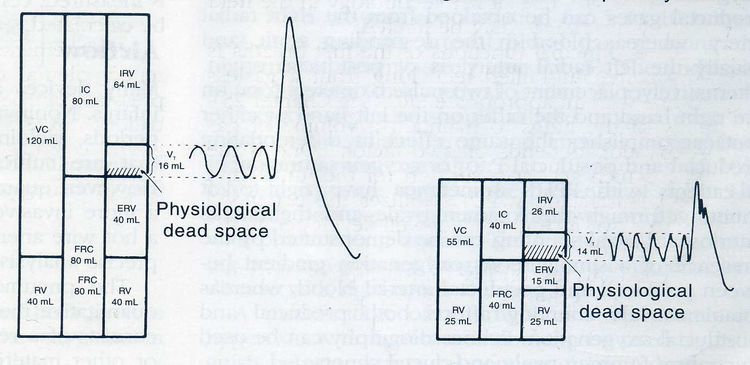
Toàn bộ thể tích khí trong phổi và đường thở có thể đo được và được chia làm các loại thể tích khác nhau (Hình 3). Kích thước của các khoang phổi liên quan với chiều cao, cân nặng và diện tích da của bệnh nhân. Dung tích khí cặn chức năng (FRC) là thể tích của khí trong các phổi có thông thương trực tiếp với đường thở cuối kỳ thở ra. Thể tích khí trong FRC có tác dụng như khoang chứa oxy trong cơ thể và hệ đệm vì vậy sự thay đổi lớn vế áp lực khí trong phế nang được giảm. Các kỹ thuật hòa loãng helium hoặc đuổi ni tơ đã được sử dụng để đo FRC ở trẻ nhỏ. Với kỹ thuật hòa loãng helium, helium cân bằng giữa thể tích và nồng độ helium đã được biết và thể tích phổi được đo. Sau khi khí được trộn lẩn và cân bằng, FRC được tính toán sử dụng nồng độ ban đầu và cuối cùng của helium và thể tích ban đầu của helium. Tương tự, FRC có thể được ước lượng bằng cách đo thể tích ni tơ bị đuổi ra khỏi phổi khi bệnh nhân hít vào không khí không có ni tơ.
Thể tích khí trong lồng ngực là toàn bộ thể tích khí trong lồng ngực vào cuối kỳ thở ra và ngược lại với FRC, bao gồm khí không có thông thương với đường thở (ví dụ: khí trong khí phế thủng mô kẽ phổi). Thể tích khí trong lồng ngực được tính bằng cách đo những sự thay đổi áp lực và thể tích trong gắng sức hô hấp chống lại đường thở bị tắc nghẽn trong khi bệnh nhân ở bên trong máy đo thể tích cơ thể. Khi gắng sức thở vào, khí trong các phổi giãn nở, thể tích phổi tăng và áp lực hoặc thể tích trong hộp tăng. Vì tích số của áp lực và thể tích là một hằng số, áp suất thay đổi trong hộp có thể được sử dụng để xác định sự thay đổi thể tích phổi, khi phân tích sự thay đổi áp lực trong đường thở tính được thể tích khí trong lồng ngực.
Thể tích khí lưu thông (VT), thể tích khí đi vào và đi ra phổi trong một nhịp thở duy nhất, có thể được đo hoặc bằng lưu tốc kế hô hấp hoặc bằng máy ghi thể tích. Dung tích sống (VC) (toàn bộ dung tích của phổi) không thể đo được ở trẻ nhỏ vì thiếu hợp tác, trừ dung tích sống khi khóc, VT trong quá trình khóc có thể đo được.
Người ta đang cố gắng đo VT từ các số đo bề mặt của sự di động thành ngực bằng cách sử dụng phép ghi biến đổi thể tích điện cảm hô hấp (RIP), RIP bao gồm hai dải băng đặt quanh bụng (AB) và lồng ngực (RC); các dải băng giãn trong lúc hít vào tương ứng những sự thay đổi diện tích cắt ngang của bụng và lồng ngực. Sự thay đổi RC và AB được cộng lại để đạt được kết quả bán định lượng của VT, khi đó VT được thể hiện như tỷ lệ phần trăm của thể tích trong giai đoạn đo 5 phút. Kỹ thuật này được phát triển vì vậy bộ phận cảm biến lưu lượng khí không còn cần được sử dụng để phát hiện ngưng thở.
RIP là một phương pháp đầy triển vọng để ước tính VT trong bối cảnh nhi khoa vì nó không cần sự hợp tác của bệnh nhân và không cần gắn thiết bị vào vị trí mặt và nó có thể được sử dụng trong thời gian dài ít gây khó chịu cho bệnh nhân. Hơn nữa, sử dụng RIP để đo VT không bị ảnh hưởng bởi vị trí của cơ thể, sự mất đồng bộ của thành ngực và tần số hô hấp. Tuy nhiên, sự thay đổi tư thế có ảnh hưởng thay đổi vào các phương pháp đo thể tích RIP phụ thuộc vào kỹ thuật đo được sử dụng. Mặc dù có thể sử dụng RIP để ghi lại những thay đổi về thông khí, phương pháp đo RIP thay đổi khi so sánh với phương pháp đo VT qua lưu tốc kế hô hấp dựa vào cơ sở nhịp thở này đến nhịp thở khác. Do những thay đổi nhỏ về VT và lưu lượng có thể tạo những sai số lớn trong các phép tính kháng lực và sự giãn nở đường thở, vai trò của kỹ thuật RIP trong lĩnh vực cơ học hô hấp có thể bị hạn chế.
Một trong những chức năng chính của những nhịp thở đầu tiên là chuyển phổi thai chứa đầy dịch từ một cơ quan không chứa khí thành một cơ quan có dung tích khí cặn chức năng (FRC) thích hợp. Khả năng của phổi để duy trì thể tích khí cuối kỳ thở ra phụ thuộc vào hai yếu tố. Một là thành ngực hoạt động như sự nâng đỡ cho phổi và yếu tố khác là surfactant ổn định các phế nang giãn ra. Cả hai yếu tố này đều kém phát triển ở trẻ đẻ non.
Trẻ 3 kg bình thường-----------------------------------------------------------------------------Trẻ 3 kg bị suy hô hấp
36 …………..………………............................... Tần số hô hấp/phút ……………......................................……………………… 70
0,3 ………………………......................... Khoảng chết/thể tích khí lưu thông ……...................................……………… 0,6
5 ……………………………............................ Áp lực trong thực quản (cm H2O) ……....................................………………. 18
4,4 ………………………...............................…… Sự giãn nỡ (mL/cm H2O) ……….....................................……………………. 1,0
29 ……………………………............................... kháng lực (cm H2O/lít/giây) ……...................................……………………. 23
40 ……………………………............................... Toàn bộ công thở/nhịp thở ……….....................................………………… 111
1440 …………………………...............................… Toàn bộ công thở/phút …………………………....................................... 7770
Hình 3: Phân chia các thể tích phổi và các trị số đo khác nhau của chức năng phổi ở một trẻ bình thường (A) và một trẻ bị bệnh màng trong (B).
Các cơ chế nguyên nhân của sự bắt đầu hô hấp có thể bao gồm các kích thích như là tiếp xúc với môi trường lạnh và những thay đổi xúc giác. Thêm vào đó, người ta đã xác định mối tương quan chính xác giữa pH, PO2 và PCO2 góp phần gây ra nhịp thở ở trẻ sơ sinh. Áp lực âm trong lồng ngực của nhịp thở đầu tiên phải vượt qua được tác động của độ nhớt của dịch trong đường thở, sức căng bề mặt và kháng lực của mô. Các nghiên cứu x quang chứng tỏ phổi phồng lên với không khí ngay trong nhịp thở đầu tiên. Sự ứ dịch phổi tạm thời có thể nguyên nhân của nhịp thở nhanh thoáng qua ở trẻ sơ sinh. Dung tích khí cặn chức năng (FRC) nhanh chóng được thiết lập, thay đổi ít trong suốt tuần lễ đầu tiên của cuộc sống.
Khoảng chết (dead space) là phần của VT không bị sự trao đổi khí ảnh hưởng, như vậy, nó thay đổi tùy thuộc vào sự xuất hiện hay không những khu vực có V ̇/Q ̇ cao. Khoảng chết được chia làm nhiều ngăn. Khoảng chết giải phẫu (anatomic dead space) là thể tích đường thở không ảnh hưởng đến sự trao đổi khí và được tạo thành bởi đường dẩn khí từ các lỗ mũi đến các tiểu phế quản tận. Khoảng chết phế nang (alveolar dead space) là thể tích của khí trong phế nang được thông khí tốt nhưng ít được tưới máu. Khoảng chết sinh lý (physiologic dead space) là tổng của khoảng chết giải phẩu và khoảng chết phế nang. Ở trẻ sơ sinh bình thường, khoảng chết sinh lý từ 6 đến 8 mL; trẻ đẻ non có giá trị nhỏ hơn. Mối liên quan giữa khoảng chết và VT bình thường khoảng 0,3. Điều quan trọng phải giảm thiểu khoảng chết do máy thông khí hổ trợ thêm vào hoặc đo các chức năng của phổi để ngăn ngừa tình trạng thở lại, tích lũy dioxide carbon (CO2) và tác động trên cùng các biến số được đo.
Áp lực[sửa]
Đo áp lực tạo cho phổi phồng lên là cần thiết để thử nghiệm chức năng phổi. Áp lực là cho phổi phồng lên có thể có được nhờ vào phương trình chuyển động:
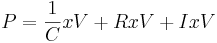 Trong
đó
P
là
áp
suất
tạo
cho
phổi
phồng,
C
là
sự
giãn
nở,
V
là
thể
tích,
R
là
kháng
lực,
V
̇
là
lưu
lượng,
I
là
quán
tính
và
V
̈
là
gia
tốc.
Thành
phần
quán
tính
thấp
và
xem
như
không
đáng
kể
trên
lâm
sàng.
Nếu
áp
lực
được
đo
khi
đường
thở
mở,
được
gọi
là
áp
lực
xuyên
hô
hấp,
các
giá
trị
sự
giãn
nở
hoặc
kháng
lực
là
những
giá
trị
của
toàn
bộ
hệ
hô
hấp.
Nếu
áp
lực
xuyên
phổi
(transpulmonary
pressure)
(áp
lực
màng
phổi
hoặc
phế
nang
trừ
áp
lực
đường
thở
mở)
được
đo,
có
thể
tính
được
sự
giãn
nở
và
kháng
lực
của
phổi.
Trong
đó
P
là
áp
suất
tạo
cho
phổi
phồng,
C
là
sự
giãn
nở,
V
là
thể
tích,
R
là
kháng
lực,
V
̇
là
lưu
lượng,
I
là
quán
tính
và
V
̈
là
gia
tốc.
Thành
phần
quán
tính
thấp
và
xem
như
không
đáng
kể
trên
lâm
sàng.
Nếu
áp
lực
được
đo
khi
đường
thở
mở,
được
gọi
là
áp
lực
xuyên
hô
hấp,
các
giá
trị
sự
giãn
nở
hoặc
kháng
lực
là
những
giá
trị
của
toàn
bộ
hệ
hô
hấp.
Nếu
áp
lực
xuyên
phổi
(transpulmonary
pressure)
(áp
lực
màng
phổi
hoặc
phế
nang
trừ
áp
lực
đường
thở
mở)
được
đo,
có
thể
tính
được
sự
giãn
nở
và
kháng
lực
của
phổi.
Đo áp lực thực quản ở trẻ nhỏ phản ánh tốt áp lực màng phổi hoặc phế nang. Có thể xác định áp lực thực quản bằng cách đặt bóng thực quản hoặc đầu catheter thực quản ở một phần ba dưới của thực quản. Khả năng theo dõi áp lực thực quản để phản ánh chính xác áp lực màng phổi hoặc phế nang nên được xác minh bằng cách thể hiện không có chênh áp giữa theo dõi áp lực đường thở và thực quản trong quá trình bít đường thở. Sự méo lồng ngực, thường gặp ở trẻ đẻ non, có thể làm giảm sự truyền áp lực màng phổi. Tuy nhiên, Coates và cộng sự đã xác định khu vực trên tim nhưng dưới cựa khí quản nơi mà sự truyền áp lực thực quản tin cậy, không phụ thuộc vào sự biến dạng thành lồng ngực.
Sự giãn nở[sửa]
Sự giãn nở là đo sự đàn hồi hoặc sự căng phồng lên (ví dụ của phổi, thành ngực hoặc hệ hô hấp) được tính từ sự thay đổi thể tích trên mỗi đơn vị thay đổi áp lực (hình 4). Sự giãn nở của hệ hô hấp bao gồm phổi và thành ngực. Ở trẻ sơ sinh, sự giãn nở phổi là thành phần quan trọng nhất, vì thành ngực rất dễ căng phồng.
Sự giãn nở phổi là sự đo độ đàn hồi bên trong của mô phổi. Sự giãn nỡ được đo hoặc là động hoặc là tĩnh tùy thuộc vào có hay không có sự giãn ra của các cơ hô hấp. Sự giãn nở phổi động được đo trong quá trình thở tự phát bằng cách sử dụng các dụng cụ đo VT và áp lực thực quản. Bằng phương pháp này, sự giãn nở phổi động được tính bằng cách chia sự thay đổi VT cho sự thay đổi áp lực giữa các điểm không có lưu lượng khí (no airflow) (có nghĩa là giữa cuối kỳ thở vào và cuối kỳ thờ ra). Tần số hô hấp cao hoặc kháng lực không cho phép áp lực cân bằng giữa các điểm không có lưu lượng và như vậy sự giãn nở động bị giảm trong những trường hợp này. Tương tự, sự giãn nở phổi tĩnh có thể được tính giữa các điểm không có lưu lượng khi các cơ hô hấp bị giãn bằng cách bít đường thở. Vì sự đàn hồi phổi tùy thuộc vào thể tích phổi, sự thay đổi FRC có thể thay đổi sự giãn nở phổi.
Hình 4: Sự giãn nở phổi (compliance) động được tính bằng ∆ thể tích/∆ áp lực được biểu hiện bằng độ dốc của đường AC. Công thở (work of breathing) được biểu hiện bằng diện tich bên trong phần được vẽ bởi ABCFA. Kháng lực (resistance) có thể được tính bằng sự thay đổi áp lực, được biểu hiện bởi sự khác biệt giữa các điểm D và B, được chia ra bởi sự thay đổi lưu lượng, được biểu hiện bằng sự khác nhau giữa các điểm G và H tại cùng các điểm giữa thể tích.
Độ đàn hồi điều chỉnh được tính bởi thể tích phổi hoặc kích thước bệnh nhân được gọi là sự giãn nở đặc hiệu. Trong khi sự giãn nở phổi đặc hiệu ở trẻ sơ sinh bình thường (1 đến 2 mL/cm H2O mỗi kilogram) tương đương với người lớn so với đơn vị cân nặng cơ thể, sự giãn nở của thành ngực tương đối cao hơn nhiều ở trẻ nhỏ.
Sự giãn nở phổi thấp lúc bắt đầu nhịp thở đầu tiên ở bất kỳ trẻ sơ sinh bình thường nào. Cùng với việc thiết lập nhịp thở và sự giảm dần dịch phổi trong 3 đến 6 giờ sau sinh, FRC tăng đồng thời với sự giãn nở phổi. Các yếu tố sinh lý bệnh có thể tăng số lượng dịch hoặc cản trở sự làm thoát dịch phổi có thể làm chậm sự giãn nở phổi. Khả năng thay đổi của các giá trị giãn nở (compliance) trong 2 giờ đầu sau sinh, một phần do sự thay đổi sinh lý, cũng có thể giải thích thường gặp tần số thở ở một số trẻ cao hơn trong giai đoạn này.
Ở những trẻ bị suy hô hấp, sự giãn nở phổi giảm đáng kể, thành ngực yếu, khi trẻ cố gắng tăng áp lực trong lồng ngực âm, thành ngực xẹp xuống (rút lõm). Thêm vào đó, đường thở của trẻ sơ sinh càng yếu càng làm cho trẻ đẻ non xẹp đường thở trong quá trình thở ra và gây bẩy khí.
Sự kháng lực[sửa]
Kháng lực phổi là đo sự ma sát gặp phải khi khí thổi qua mũi hầu, khí quản và phế quản và do mô di chuyển vào mô. Định nghĩa cơ bản của tình trạng kháng lực:
Kháng lực=∆Áp lực/∆Lưu lượng
Độ
dẩn
(conductance)
là
hàm
nghịch
đảo
của
kháng
lực.
Kháng
lực
phụ
thuộc
vào
đường
kính
đường
thở,
các
đặc
tính
của
mô
và
tần
số
lưu
lượng.
Kháng
lực
phổi
ở
trẻ
sơ
sinh
đủ
tháng
khoảng
30
cm
H2O/L
mỗi
giây,
cao
hơn
người
lớn
xấp
xỉ
sáu
lần.
Cả
hai
kháng
lực
đường
thở
(kháng
lực
do
đường
thở
tạo
ra)
và
kháng
lực
nhầy
(kháng
lực
do
các
mô
tạo
ra
góp
phần
tạo
kháng
lực
phổi
toàn
bộ.
Do kháng lực cao ở trẻ nhỏ, nên sử dụng các dụng cụ hô hấp có kháng lực nhỏ. Vị trí chính của kháng lực đường thở ở trẻ sơ sinh là đường thở trên, đặc biệt là các lỗ mũi. Kháng lực cao của đường thở trên làm hạn chế khả năng phát hiện những thay đổi nhỏ trong kháng lực phổi.
Công thở[sửa]
Công thở là một phép đo năng lượng cần để làm phồng phổi và di chuyển thành ngực. Trong thuật ngữ chung, công là tích số lũy tiến của áp lực và thể tích khi di chuyển ở mỗi bệnh nhân. Ở trẻ bình thường, toàn bộ công hô hấp được xác định một giá trị trung bình 1440 g.cm mỗi phút. Ở một trẻ bị suy hô hấp, công thở toàn bộ tăng sáu lần.
Điều này quan trọng nhất khi xem xét oxy cho trẻ thở. Trẻ sơ sinh cần tiêu thụ calo cao hơn để thở so với người lớn và trẻ suy hô hấp cần phải tiêu thụ nhiều calo hơn cho chức năng này. Ở trẻ đủ tháng, công thở tối thiểu khi trẻ có tần số hô hấp 30 lần mỗi phút.
XEM THÊM[sửa]
- Bệnh màng trong
- Các thuốc sử dụng phối hợp trong Thở máy Sơ sinh
- Tăng áp phổi tồn tại sơ sinh
- Nhi khoa
- Sơ sinh
- Dịch và các chất điện giải trẻ Sơ sinh
- Lịch Tiêm chủng
- Vàng da Sơ sinh
- Vàng da tăng bilirubin máu
TÀI LIỆU THAM KHẢO[sửa]
- Fanaroff and Martin’s. Neonatal-Perinatal Medicine. 8th Edition. Elsevier Mosby. 2006. Volume two: Diseases of the Fetus and Infant. Blood gases. 1088-1097
- Dean R. Hess; Robert M. Kacmarek. Những vấn đề thiết yếu trong thông khi cơ học. (Esssential of Mechanical Ventilation). Nhà Xuất Bản Đà Nẵng. 2005. BS. Lê Hồng Hà; Nguyễn Huỳnh Điệp dịch
Bài liên quan
Liên kết đến đây
- Tủ sách Khoa học
- Bản mẫu:Sách mới
- Các thuốc sử dụng phối hợp trong thở máy sơ sinh
- Thành viên:Võ Đức Minh
- Bệnh màng trong
- Chăm sóc trẻ sơ sinh
- Sơ sinh
- Nhi khoa
- Tăng áp phổi tồn tại sơ sinh
- Vàng da sơ sinh
- Xem thêm liên kết đến trang này.