Giải Nobel sinh lý học và y học năm 2007
Thông cáo báo chí
16 giờ 30, ngày 8-10-2007
Hội đồng xét giải Nobel tại viện Karolinska Thụy Điển hôm nay quyết định trao giải Nobel Sinh lý học và Y học 2007 cho
Mario R. Capecchi, Martin J. Evans và Oliver Smithies
Về những khám phá ra "nguyên lí gây biến đổi gene đặc hiệu ở chuột bằng cách sử dụng các tế bào gốc phôi" (principles for introducing specific gene modifications in mice by the use of embryonic stem cells).
Tóm tắt[sửa]
Những người đoạt giải Nobel năm nay đã thực hiện một loạt các khám phá nền tảng liên quan tới tế bào nguồn tạo phôi (ES cells) và tái tổ hợp DNA ở động vật có vú. Những khám phá của họ đã tạo ra một kĩ thuật ưu việt được gọi là "nhắm đích gen" (gene targeting) ở chuột. Hiện tại nó đang được ứng dụng trong hầu hết các lĩnh vực của y sinh học - từ nghiên cứu cơ bản đến sự phát triển các liệu pháp mới.
Định hướng gene thường được sử dụng để làm bất hoạt một gene đơn lẻ. Những thí nghiệm "bất hoạt" (knockout") gene như thế đã và đang giải thích vai trò của số lớn các gene trong quá trình phát triển phôi, sinh lý phát triển, lão hóa và bệnh tật. Đến hôm nay, trên mười ngàn gene chuột (xấp xỉ một nửa số gene trong hệ gene động vật có vú) đã có thể bị bất hoạt. Những nỗ lực quốc tế nhằm tạo ra ngân hàng chuột "knock-out" với tất cả các gene có thể trở thành hiện thực trong một tương lai gần.
Bằng phương pháp nhắm đích gene, hiện nay người ta có thể tạo ra hầu hết các loại biến đổi DNA ở hệ gene chuột, điều này cho phép các nhà khoa học xác định vai trò của từng gene riêng lẻ đối với bệnh tật và sức khỏe. Nhắm đích gene đã tạo ra hơn 500 mô hình khác nhau trên chuột mang các dị tật của người, bao gồm chứng thoái hóa thần kinh, tim mạch, tiểu đường và ung thư.
Nội dung[sửa]
Biến đổi gene bằng tái tổ hợp tương đồng
Thông tin quy định quá trình hoạt động và phát triển của cơ thể trong suốt cuộc đời được mã hóa trong DNA. Các phân tử DNA được lưu trữ trong những cặp nhiễm sắc thể, mà trong mỗi cặp có một nhiễm sắc thể nhận từ cha và chiếc còn lại nhận từ mẹ. Những đoạn DNA trên cặp nhiễm sắc thể có thể đổi chỗ cho nhau trong quá trình tái tổ hợp tương đồng (homologous recombination). Đây chính là nhân tố làm tăng đa dạng di truyền trong quần thể và được bảo tồn xuyên suốt quá trình tiến hóa của sinh giới. Cơ chế tái tổ hợp tương đồng đã được phát hiện đầu tiên ở vi khuẩn hơn 50 năm về trước bởi Joshua Lederberg, người đoạt giải Nobel Y học năm 1958.
Cả Mario Capecchi và Oliver Smithies đã có ý tưởng lợi dụng cơ chế tái tổ hợp tương đồng để sửa đổi một cách đặc hiệu các gene ở tế bào động vật có vú và họ đã thực hiện hàng loạt công trình để phát triển ý tưởng này.
Capecchi đã chứng minh bằng thực nghiệm rằng tái tổ hợp tương đồng có thể xảy ra trong tế bào đông vật có vú giữa đoạn DNA ngoại lai và nhiễm sắc thể của tế bào vật chủ. Ông đã cho thấy rằng các gene khiếm khuyết có thể được sửa lại thông qua sự tái tổ hợp tương đồng bằng cách đưa vào tế bào những đoạn DNA lành lặn. Smithies là người đầu tiên đã thử sửa sai các gene đột biến ở tế bào người. Ông nghĩ rằng một số bệnh di truyền về máu có thể chữa trị được bằng cách sửa chữa các đột biến gây bệnh tại những tế bào nguồn tủy xương. Trong quá trình nghiên cứu, Smithies đã khám phá ra rằng các gene nội sinh của cơ thể cũng có thể bị điều khiển hoạt động một cách bất thuận nghịch thông qua cơ chế này. Điều này cho thấy rằng tất cả các gene đều có thể bị biến đổi đặc hiệu thông qua kỹ thuật tái tổ hợp tương đồng.
Tế bào nguồn tạo phôi ở chuột có thể trở thành tế bào nguồn dòng tinh
Các loại tế bào ban đầu được Capecchi và Smithies nghiên cứu đã không thể tạo nên những cơ thể động vật biến đổi gene. Điều này đòi hỏi những nhà khoa học phải tìm ra một loại tế bào khác có thể phát triển thành tế bào sinh giao tử (tế bào dòng tinh). Chỉ với loại tế bào này, các biến đổi gene mới có khả năng di truyền tạo nên những thế hệ cơ thể mang biến đổi gene.
Martin Evans đã làm việc nhiều năm với các tế bào nguồn ung thư ở chuột (EC), đây là các tế bào được lấy từ những khối u và có thể biệt hóa thành nhiều loại tế bào. Ông đã có ý tưởng sử dụng tế bào EC để mang những biến đổi gene vào trong tế bào dòng tinh ở chuột. Cố gắng của ông ban đầu không thành công bởi vì các tế bào EC mang nhiễm sắc thể bất thường đã không thể sản sinh tinh trùng. Trong quá trình tìm kiếm giải pháp thay thế, Evans phát hiện ra rằng người ta có thể thiết lập các dòng tế bào nuôi cấy có nhiễm sắc thể bình thường từ chính những tế bào phôi chuột ở giai đoạn đầu. Những tế bào loại này hiện nay được gọi là tế bào nguồn tạo phôi (ES).
Các nghiên cứu sau đó theo hướng này đã cho thấy tế bào ES có thể tạo nên các tế bào dòng tinh (xem hình trên). Người ta đã tiêm tế bào ES của một chủng chuột vào phôi của một chủng chuột khác. Các phôi khảm này (chú thích, mang tế bào của cả hai chủng chuột) được cấy vào một con chuột me mang thai. Những con chuột sinh ra là những thể khảm và sau đó được lai với nhau để kiểm tra sự hiện diện những gene đặc trưng của tế bào ES trên thế hệ chuột tiếp theo. Những gene này sau đó được di truyền theo các định luật Mendel.
Sau đó Evans đã bắt đầu tìm cách thay đổi gene của các tế bào ES. Để thực hiện mục đích này ông đã chọn retrovirus, loại virus có thể sát nhập gene của chúng vào trong nhiễm sắc thể. Ông đã chứng mình bằng thực nghiệm sự vận chuyển DNA của retrovirus từ tế bào ES, thông qua chuột khảm, vào trong tế bào dòng tinh của thế hệ chuột sau đó. Như vậy, Evans đã sử dụng các tế bào ES để tạo ra những con chuột mang biến đổi di truyền.
Hai ý tưởng lớn gặp nhau - tái tổ hợp tương đồng ở tế bào ES
Vào năm 1986 mọi tiền đề để tạo nên những tế bào ES mang gene bị biến đổi bằng cơ chế định hướng gene đã sẵn sàng. Capecchi và Smithies trước đó đã chứng minh các gene trong tế bào nuôi cấy có thể bị biến đổi thông qua tái tổ hợp tương đồng, và Evans đã tạo nên cách thức cần thiết để tạo ra tế bào tinh trùng chuột - đó là tế bào ES. Bước tiếp theo là kết hợp hai công trình này lại.
Trong những thí nghiệm đầu tiên, cả Capecchi và Smithies chọn gene hprt, vì gene này dễ phát hiện. Đây là gene liên quan đến một bệnh di truyền hiếm gặp ở người (hội chứng Lesch-Nyhan). Capecchi đã cải tiến kỹ thuật định hướng gene và phát triển một phương pháp chọn lọc mới (chọn lọc có - không, xem hình) có tính khả dụng cao.
Con chuột "knock-out" đầu tiên chào đời - sự bắt đầu của một kỉ nguyên mới trong di truyền học
Những công trình đầu tiên sử dụng kỹ thuật tái tổ hợp tương đồng ở tế bào ES để tạo ra những con chuột biến đổi gene được công bố vào năm 1989. Kể từ đó những công trình tạo ra các chủng chuột bị bất hoạt gene đã gia tăng theo cấp số nhân. Định hướng gene đã phát triển thành một kĩ thuật có tính khả dụng cao. Giờ đây những nhà khoa học đã có thể tạo ra những cơ thể mang các đột biến được hoạt hóa tại thời điểm nhất định, hoặc chỉ hoạt động trong những tế bào/cơ quan nhất định trong quá trình phát triển.
Định hướng gene được sử dụng để nghiên cứu sức khỏe và bệnh tật
Những nhà khoa học có thể áp dụng kỹ thuật định hướng gene để nghiên cứu hầu như mọi quá trình sinh lý ở động vật có vú. Ngày nay chúng ta đã và đang chứng kiến một sự bùng nổ các hoạt động nghiên cứu ứng dụng kĩ thuật này. Định hướng gene hiện nay đã được quá nhiều nhóm nghiên cứu sử dụng và được mô tả trong nhiều công trình mà người ta khó có thể tóm tắt ngắn gọn được. Do đó, một vài công trình gần đây của những người đoạt giải Nobel năm nay được chọn lọc để liệt kê dưới đây.
Định hướng gene giúp chúng ta thấu hiểu vai trò của hàng trăm gene trong quá trình phát triển bào thai động vật có vú. Nghiên cứu của Capecchi tiết lộ vai trò của những gene liên quan trong quá trình phát triển cơ quan và trong cơ chế thiết lập hình trạng cơ thể ở động vật có vú. Công trình của ông đã làm sáng tỏ nguyên nhân của hàng loạt bệnh tật/dị tật bẩm sinh ở người.
Evans đã ứng dụng định hướng gene để xây dựng mô hình chuột cho các bệnh ở người. Ông đã phát triển hàng loạt mô hình cho bệnh u xơ nang di truyền ở người, sử dụng những mô hình này để nghiên cứu cơ chế gây bệnh và kiểm tra hiệu quả của những liệu pháp gene.
Smithies cũng đã sử dụng định hướng gene để phát triển mô hình chuột cho những bệnh di truyền chẳng hạn như u xơ nang, chứng thiếu máu. Ông cũng đã phát triển một số lớn chuột mô hình cho những bệnh thông thường ở người chẳng hạn cao huyết áp và xơ vữa động mạch.
Tóm lại, định hướng gene ở chuột đã tràn ngập mọi lĩnh vực của y sinh học. Ảnh hưởng của nó tới sự thấu hiểu chức năng gene và những lợi ích của nó đối với nhân loại sẽ tiếp tục gia tăng trong nhiều năm nữa.
Tiểu sử[sửa]
Mario Capecchi sinh năm 1937 ở Ý, công dân Mỹ, PhD in Biophysics 1967, Harvard University, Cambridge, MA, USA. Howard Hughes Medical Institute Investigator và Distinguished Professor of Human Genetics và Biology at the University of Utah, Salt Lake City, UT, USA.
Sir Martin J. Evans, sinh năm 1941, Great Britain, công dân Anh, PhD in Anatomy and Embryology 1969, University College, London, UK. Director of the School of Biosciences và Professor of Mammalian Genetics, Cardiff University, UK.
Oliver Smithies, sinh 1925 ở Great Britain, công dân Mỹ, PhD in Biochemistry 1951, Oxford University, UK. Excellence Professor of Pathology và Laboratory Medicine, University of North Carolina at Chapel Hill, NC, USA.
Nguồn[sửa]
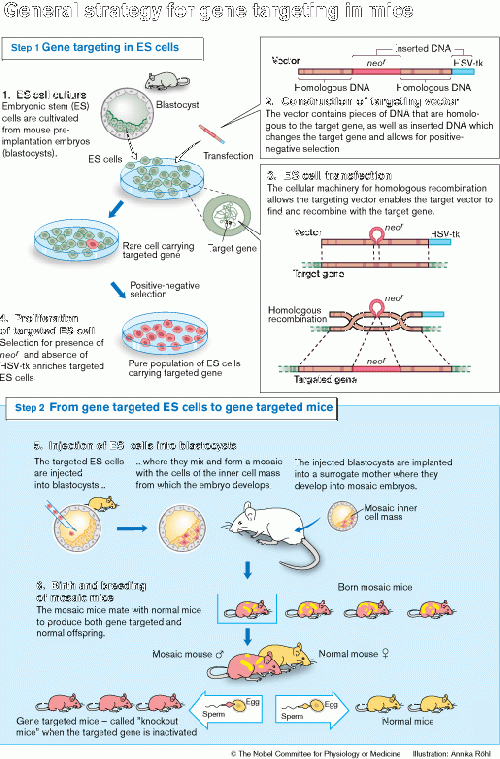
Chú thích hình - Sơ đồ tổng quát kỹ thuật định hướng gene ở chuột[sửa]
Bước 1. Định hướng gene vào tế bào ES
1. Canh trường tế bào ES. Tế bào nguồn tạo phôi (ES cell) được tách ra từ túi phôi (blastocyst)
2. Cấu trúc của vector định hướng (targeting vector). Vector định hướng chứa 1) các đoạn DNA có trình tự tương đồng với trình tự của gene đích (target gene), 2) đoạn DNA bổ sung (nd. đoạn neo r) làm thay đổi gene đích và cho phép chọn lọc có - không.
3. Gây nhiễm tế bào ES. Cơ chế tái tổ hợp tương đồng của tế bào sinh vật đã cho phép vector định hướng có thể tìm thấy gene đích và bổ sung đoạn DNA mới vào vị trí của gene đích.
4. Nuôi cấy chọn lọc tế bào ES mang biến đổi di truyền (targeted ES cell) Sự hiện diện của đoạn neo r và không có mặt HSV - tk là tiêu chí để chọn lọc trong quá trình làm giàu tế bào ES mang biến đổi di truyền.
(nd. Tế bào ES mang biến đổi di truyền trong hình có màu hồng. Tế bào nhân đỏ là loại tế bào mang gene định hướng, ban đầu có số lượng rất ít. Thông qua chọn lọc có - không, những tế bào nhân đỏ sẽ tăng trưởng thành quần thể tế bào thuần chủng mang gene định hướng.)
Bước 2. Từ tế bào ES biến đổi di truyền đến những cơ thể chuột đột biến gene.
5. Tiêm tế bào ES vào túi phôi
Các tế bào ES mang biến đổi di truyền được tiêm vào túi phôi, nơi chúng được trộn lẫn và tạo ra thể khảm với các tế bào nút phôi (inner cell mass) trong quá trình phát triển của phôi. Các túi phôi đã tiêm tế bào ES được cấy vào một con chuột mang thai để có thể phát triển thành phôi khảm (mosaic embryo).
(Mosaic inner cell mass: Các tế bào nút phôi không đồng nhất (khảm))
6. Sự sinh sản và chọn giống của chuột khảm.
Chuột khảm được lai với chuột bình thường để tạo những con chuột bình thường và một số chuột con bị biến đổi di truyền (nd. chuột màu đỏ).
(nd. Trong hình chuột khảm đực được lai với chuột cái bình thường. Tinh trùng mang biến đổi gene khi thụ tinh với trứng bình thường đã cho đời con là những con chuột biến đổi gene, tinh trùng bình thường thụ tinh với trứng bình thường cho đời con lai là chuột bình thường.)
Chuột mang biến đổi di truyền tạo ra từ kỹ thuật định hướng gene được gọi chuột knock-out khi việc định hướng gene làm bất hoạt gene đích.
Xem thêm[sửa]
- Nobel Y học 2007 tôn vinh nghiên cứu tế bào gốc trên Vietnamnet
- Ba nhà khoa học Anh - Mỹ thắng Giải Nobel Y học trên Tuổi trẻ
- Nobel Y học cho công trình nghiên cứu gen trên BBC tiếng Việt
- Gene knock-out, knock-in và knock-down